INTRODUCCIÓN
El virus de la bronquitis infecciosa (IBV) causa una enfermedad del tracto respiratorio superior altamente contagiosa en los pollos, además de graves pérdidas económicas en la industria avícola de todo el mundo. El agente etiológico es un coronavirus aviar. Entre las proteínas estructurales del IBV, la subunidad S1 de la glicoproteína espiga es responsable de la unión a la membrana celular del huésped, así como también, de la inducción de la neutralización y la hemaglutinación de los anticuerpos inhibidores. Además, las variaciones de aminoácidos en S1 han dado como resultado muchos serotipos diferentes de IBV. Por lo tanto, ahora se sabe que la mayoría de los países poseen sus propias variantes indígenas. La aparición de nuevas cepas variantes complica el control de la enfermedad.
OBJETIVO
Evaluar las características clínicas y patológicas, aislar e identificar la cepa circulante de IBV a partir de casos clínicos en pollos de engorde en Perú.
MATERIALES Y MÉTODOS
Caso:
En diciembre del 2015 se recibieron diez pollos entre machos y hembras de 33 y 30 días de edad provenientes de dos granjas distantes (denominadas A y B) en el norte de la ciudad de Lima. Las aves fueron vacunadas el día 1 de edad contra IBV, cepas MA5 y H120.
Aislamiento del virus:
Se tomaron muestras separadas por duplicado de tráqueas y pulmones, tonsilas cecales y riñones. Las muestras se inocularon en huevos SPF, se evaluó a los embriones y se recolectó el líquido alantoideo.
PCR y genotipificación:
Para la codificación de la región S1, los genes se amplificaron usando un RT-PCR estándar (5), la purificación se llevó a cabo usando un kit de extracción. El árbol filogenético se generó utilizando el método Neighbor-Joining en el software MEGA versión 7.
RESULTADOS
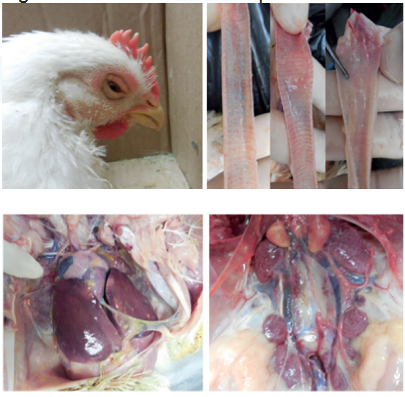
Los pollos mostraron dificultad respiratoria, tos, secreción ocular/nasal y depresión. En la necropsia se observó congestión y presencia de mucosidad en las tráqueas, aerosaculitis y riñones congestionados sin depósito de uratos (Figura 1).
Figura 1. Lesiones macroscópicas
Aislamiento
La mortalidad embrionaria registrada en las primeras 24h post-inoculación se consideró no específica. En el tercer pasaje, después de 7 días, se observó que IBV causó embriones con retraso de crecimiento, enanos, encorvados y congestionados (Figura 2 y 3).
Figura 2. Embriones infectados
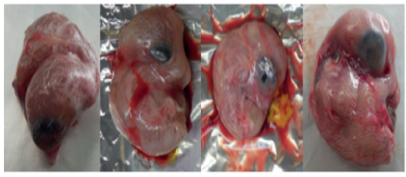
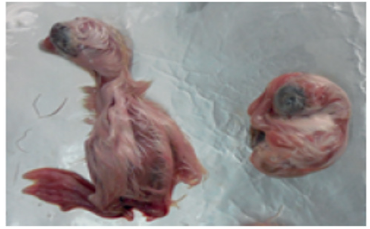
Figura 3. Embrión control vs embrión infectado
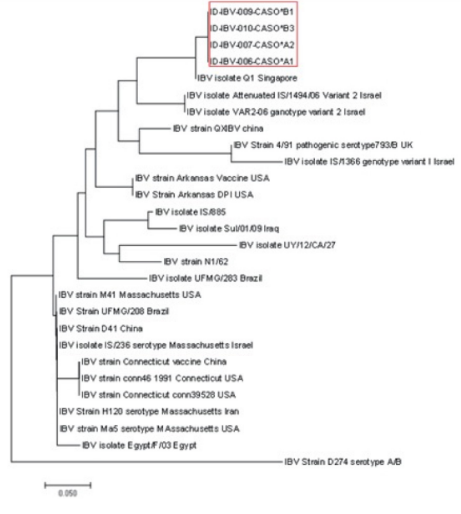
Las ramas del árbol filogenético muestran el porcentaje en el que se agrupan los taxones asociados (Figura 4). El árbol se ha dibujado a escala, en el que la longitud de los brazos se basa en el número de sustituciones por sitio. El análisis incluye 24 secuencias de referencia, cada una representada por su serotipo y especie.
Figura 4. Árbol filogenético
CONCLUSIÓN
Se logró identificar la cepa Q1 a partir de las tonsilas cecales, tráquea y pulmones de las aves de la granja A; y a partir de riñones, tráquea y pulmón de la granja B. Con estos resultados se concluye que en el Perú circula la cepa variante Q1.
OBJETIVO.
El objetivo del estudio es producir un inóculo viral inactivado de Adenovirus aviar serotipo 8b (FAdV-8b) usando células LMH como plataforma de cultivo.
MATERIALES Y MÉTODOS
Línea Celular y virus.
Célula de hepatoma de pollo (LMH) cultivada a 37°C y 5% de CO2 en medio DMEM, con 10% de Suero Bovino Fetal (SBF). Virus FAdV-8b fue aislado desde una granja de pollos de engorde.
Producción de FAdV-8b.
LMH al 70 % de confluencia fueron infectados con FAdV-8b a un MOI de 10 y se incubó a 37°C y 5% de CO2; 96 h después, se cosechó y centrifugó a 4000 RPM por 30 min a 4°C. Luego, el sobrenadante fue filtrado en 0,22 µm.
Titulación de FAdV-8b mediante TCID50.
En placa de 96 pozos fue sembrado con 3,0 x 104 células, en 100 µL de medio DMEM con 10% de SBF y se incubó a 37°C y 5% de CO2 por 8 h. Luego, se prepararon diluciones seriadas del virus desde 10-1 hasta 10-10, y 100 µL de cada dilución fue adicionada en los pozos, 8 réplicas por cada dilución. La placa fue incubada a 37°C en 5% de CO2 por 7 días. Se contó el número de pozos infectados y se realizó el cálculo del título viral por TCID50
La Figura 2 muestra la evolución del título viral en el cultivo de LMH, alcanzando un título viral máximo a las 96 hpi: 4,7 x 108 TCID50/mL. Se observó que las muestras virales tratadas con BEI no causaron alteración de la morfología o monocapa de las células LMH (Figura 3A), y presentaron similares características a cultivos control negativo de infección (Figura 3C). Las muestras virales sin tratamiento BEI (Figura 3B) causaron alteración de la morfología y pérdida total de la monocapa, de manera similar al control positivo (Figura 3D). Por tanto, la muestra tratada con BEI perdieron su capacidad de infectar y se considera inóculo viral inactivo.
CONCLUSIONES
Se alcanzó un título de FAdV-8b de 4,7 x 108 TCID50/mL, que fue inactivada con BEI exitosamente, lo cual le confiere a este producto un gran potencial para uso en vacuna. Se ha establecido un método estandarizado para la obtención de un inóculo viral inactivado para una potencial vacuna FAdV-8b que alcanzó un título viral mayor a 108 TCID /mL
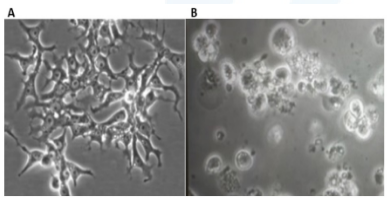
Figura 1. Cambios morfológicos de células LMH en ausencia (A) o presencia de FAdV- 8b.
Inactivación con BEI.
Se preparó etilenimina binaria (BEI) de una mezcla de 0,58M de bromhidrato de 2-bromoetilamina y NaOH de 0,5M, incubada a 37°C por 1 h. BEI se añadió a la suspensión viral (concentración final 29 mM) y se incubó a 100 rpm, a 37°C por 18h. Luego, se adicionó una solución de tiosulfato de sodio 1,26 M, 10% del volumen del BEI usado, para neutralizar el BEI residual
Pérdida de Infectividad.
Muestras virales (tratadas y no tratadas con BEI) fueron inoculadas en cultivos LMH al 70% de confluencia. Se retiró el sobrenadante, y 0,5 mL de muestra viral fue adicionada en la monocapa de células y se incubó por 1h a 37°C. Luego, se adicionó medio DMEM con 10 % SBF e incubó a 37°C y 5% de CO2 por 7 días. Ausencia de efecto citopático se consideró como pérdida de infectividad. Como control negativo se usó un cultivo LMH sin adición de virus.
RESULTADOS
A las 72 hpi (Figura 1B), se observó pérdida casi total de la morfología y monocapa celular, gran cantidad de cuerpos celulares en suspensión y restos celulares.
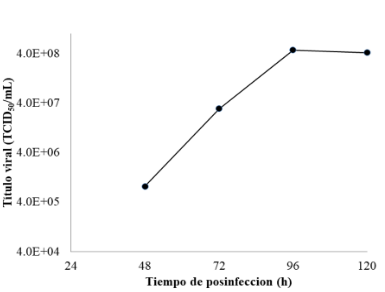
Figura 2. Evolución de carga viral
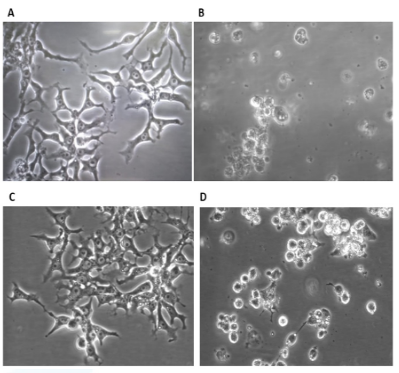
Figura 3. Cambios morfológicos microscópicos de células LMH con FAdV-8b tratado con BEI (A), o inoculado con FAdV-8b sin tratamiento BEI (B). Control negativo, cultivo LMH en ausencia de FAdV-8b (C). Control positivo, cultivo LMH en presencia de FAdV-8b (D).
OBJETIVO
El objetivo del estudio fue caracterizar la presencia del gen de la fibra de los serotipos de FAdV-4, 8b y 11 mediante la optimización de la Reacción en Cadena de la Polimerasa Múltiple (PCRm).
MATERIALES Y MÉTODOS
Extracción de ADN.
Se extrajo el ADN de 20 aislamientos de Hepatitis por Cuerpos de Inclusión, recolectados de diferentes granjas avícolas peruanas entre los años 1998 al 2021. Para la optimización de la PCRm se utilizaron tres muestras previamente identificadas como FAdV-4, 8b y 11.
Diseño de cebadores específicos.
Se seleccionaron secuencias idénticas de la fibra para cada serotipo en el Basic Local Alignment Search Tool (BLAST), para luego ser alineadas mediante el programa Clustal Omega (v. 2.0.12). Se seleccionaron regiones conservadas entre el mismo serotipo, pero que a su vez no presenten identidad con las secuencias de los otros serotipos evaluados. En base a estas secuencias se diseñaron los cebadores (sentido y antisentido) y se sintetizaron en un laboratorio externo (Integrated DNA Laboratory, EEUU).
Optimización de la PCRm.
Se sometieron los tres juegos de cebadores y los tres ADN identificados en una sola reacción. Se trabajaron con d i s t i n t a s condiciones, determinándose optimizada la
RESULTADOS
Diseño de cebadores específicos.
Se obtuvo un porcentaje de identidad entre 90- 100% de cada cebador frente a serotipos de su misma especie, y sin interferencia con otras especies de virus aviares. Se obtuvieron las secuencias de nucleótidos de los cebadores (datos por publicar) con un tamaño esperado de 1186 bp, 978 bp y 1655 bp para FAdV- 4, FAdV-8b y FAdV-11, respectivamente.
Optimización de la PCRm.
En la Figura 1 se visualizaron simultáneamente los productos definidos e intensos del tamaño esperado para cada serotipo.

Figura 1. Electroforesis de la PCRm optimizada. M: marcador; P: PCRm con tres templados (FAdV-4, 8b y 11); B: control sin ADN (agua ultrapura).
Evaluación de las muestras mediante la PCRm.
Se caracterizaron los serotipos 4, 8b y 11; de los cuales 11 muestras (55%) fueron positivas a FAdV-4, 6 (30%) a FAdV-8b y 2 (10%) a
FAdV-11. Asimismo, se observó la presencia de una coinfección entre FAdV-4 y FAdV-11 (5%) (Figura 2).
La muestra de coinfección entre FAdV-4 y
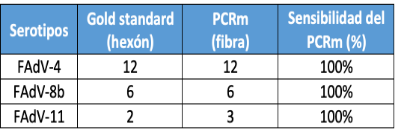
11 fue tomada como positiva para ambos serotipos al comparar los resultados de la PCR múltiple frente al secuenciamiento por el gen del hexón. Se determinó un 100% de sensibilidad de la PCRm frente a la prueba de referencia (Cuadro 1)
PCRm al emplear 0.94X de concentración final de PCR Master Mix 2x (Promega corporation, EEUU), 5.18 mM de concentración final del ión magnesio (Mg2+), 0.37 µM de concentración final de cada cebador y, 7.54 a 15.09 ng/µL de concentración final de cada ADN. El termociclador fue programado con una desnaturalización inicial de 3 min a 95°C; 20 ciclos de desnaturalización de 1 min a 95°C, alineamiento de 1 min a 54°C y extensión de 1 min 30 s a 72°C, seguido de una extensión final de 10 min a 72°C. Los productos fueron separados por electroforesis en 0.9% de gel de Agarosa sumergido en buffer Tris-acetate-EDTA (TAE) a una concentración de 1X a 120 voltios por 70 minutos.
Evaluación de las muestras mediante la PCRm.
Se realizó la reacción de PCRm para cada ADN extraído empleando como control positivo a las muestras previamente identificadas, y como control negativo a agua ultrapura. Las 20 muestras fueron secuenciadas en base al gen del hexón en el Poultry Diagnostic and Research Center (PDRC) de la Universidad de Georgia en EEUU, para determinar la sensibilidad de la PCRm optimizada frente a la prueba de referencia (gold estandard).
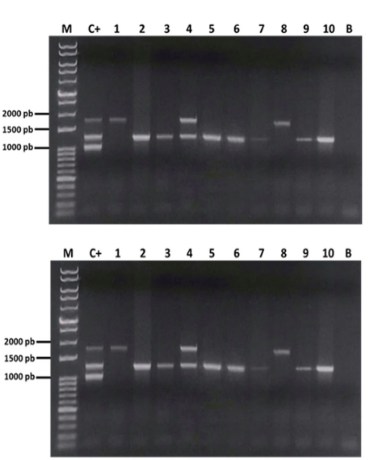
Figura 2. Electroforesis de la PCRm de las 20 muestras. M: marcador; C+: control positivo de ADNp; carril 1 al 20: muestras; B: control negativo.
Cuadro 1. Sensibilidad de la PCR multiplex frente al secuenciamiento.
4. CONCLUSIONES
Es el primer estudio de caracterización molecular de FAdV-I (FAdV-4, 8b y 11) mediante una PCR múltiple. Esta alternativa diagnóstica permitió reducir el tiempo de trabajo y de entrega de resultados, así como aminorar costos de laboratorio. Asimismo, la PCRm se puede emplear como herramienta de vigilancia epidemiológica para facilitar la implementación de programas específicos de vacunación, o como control de calidad en la identificación de inóculos virales en plantas de producción de vacuna.
INTRODUCCIÓN
Los adenovirus aviares (FAdV) tienen una distribución mundial y se han agrupado en 5 especies (A-E) con 12 serotipos: 1-8a a 8b-11. El hexón del adenovirus contiene determinantes antigénicos, la región del bucle hexón 1 (L1), representa la región más variable y, cuando se usa en la PCR junto con la secuenciación del ADN o el análisis de enzimas de restricción, fue exitoso para identificar y diferenciar algunos o todos los 12 serotipos de FAdV. Los FAdV causan hepatitis por cuerpos de inclusión, síndrome de hidropericardio, erosión de la molleja y necrosis pancreática. El grado variable de mortalidad se correlaciona con la patogenicidad del virus, los diferentes serotipos de la cepa infectante y la susceptibilidad de los pollos. La identificación de los serotipos involucrados es significativa para el rastreo epidemiológico y es de importancia crítica en la vacunación para el control de la enfermedad.
OBJETIVO
Evaluar las características clínicas y patológicas, aislar e identificar los serotipos circulantes de FAdV a partir de casos clínicos de Hepatitis por Cuerpos de Inclusión (HCI) en pollos de engorde de Perú.
MATERIALES Y MÉTODOS
Caso
El laboratorio de I+D recibió hígados congelados y pollos comerciales vivos sospechosos de HCI adquirida provenientes de diferentes departamentos de la costa peruana entre el 2015 y 2016. Los pollos afectados mostraron un crecimiento desigual, depresión y plumas erizadas.
Examen histopatológico
Las muestras de hígado se fijaron en formalina neutra al 10% durante 48 horas a temperatura ambiente. Los tejidos se procesaron de forma rutinaria, se incrustaron en cera parafina y se cortaron en secciones de 5 µm. Las secciones se tiñeron con hematoxilina y eosina (H&E), y se examinaron las lesiones asociadas con la infección por FAdV mediante microscopía óptica.
RESULTADOS
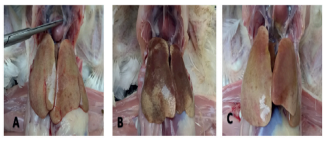
Durante la examinación post-mortem, se observó lesiones macroscópicas de HCI principalmente en el hígado, que presentó hepatomegalia (A, B, C) y coloración amarillo pálido (A, B) (Figura 1). Otras muestras se recibieron congeladas y no fue posible evaluar las lesiones. Las imágenes pertenecen a la muestra ID-HCI-032.
Figura 1. Lesiones macroscópicas en hígado
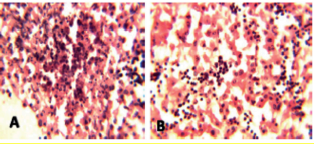
La evaluación histopatológica de las muestras mostró diversos grados de picnosis y cariorrexis (A), y cuerpos de inclusión intranucleares con marginación de la cromatina
(B) (Figura 2). También se presentaron múltiples hemorragias subcapsulares, grupos multifocales de hepatocitos y degeneración lipídica.
Figura 2. Histopatologia de hígados
Patogenicidad: Durante la primera semana post-inoculación, no se registró mortalidad en los pollos inoculados con FAdV-7;
PCR y genotipificación
Se detectó adenovirus en todas las muestras mediante PCR en tiempo real (4); la determinación de serotipos se realizó mediante secuenciación de la región L1 del gen hexón. El árbol filogenético se generó mediante el método Neighbor-Joining utilizando el software MEGA versión 7: Molecular Evolutionary Genetics Analysis versión
7.0 para conjuntos de datos más grandes.
Evaluación de patogenicidad en pollos SPF
Se utilizaron 100 pollos SPF de 10 días de edad para determinar el potencial patogénico de dos FAdV. Los pollos se dividieron aleatoriamente en cinco grupos de 20 aves cada uno. Se les inoculó por vía subcutánea con 104 EID de una de las 2 cepas de los serotipos 4 o 7, aisladas de las muestras.
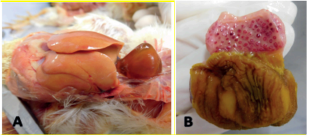
mientras que los pollos inoculados con FAdV-4 presentaron una alta mortalidad (65%). Al 4º día post-inoculación, estos pollos evidenciaron depresión, hepatitis (A), proventrículo hemorrágico (B), y molleja dañada (Figura 3). Las imágenes pertenecen al serotipo 4, muestra ID-HCI-036.
Figura 3. Lesiones macroscópicas en hígado y proventrículo
Genotipificación: Las ramas del árbol filogenético muestran el porcentaje en el que se agrupan los taxones asociados (Figura 4). El árbol se ha dibujado a escala, en el que la longitud de los brazos se basa en el número de sustituciones por sitio. El análisis involucra 21 secuencias de referencia, cada una representada por su serotipo y especie
Figura 4. Árbol filogenético

CONCLUSIÓN
En conclusión, los serotipos 4 y 7 (bajo la clasificación ICTV) se encuentran circulando en casos clínicos de HCI en el Perú. El serotipo 4 presenta alta mortalidad, mientras que el serotipo 7 no presenta mortalidad.
OBJETIVO
El objetivo del presente estudio fue evaluar, bajo condiciones experimentales, la protección e inocuidad de la vacuna inactivada gelificada Inmuno Broiler® de Quimtia S.A contra la Enfermedad de Newcastle (ENC) en pollos SPF.
MATERIALES Y MÉTODOS
Lugar y fecha de estudio
El estudio se realizó en el Laboratorio de Patología Aviar de la Facultad de Medicina Veterinaria de la UNMSM, durante el 13 de
agosto hasta el 11 de octubre del 2015.
Animales
Se usaron 80 pollos libres de patógenos específicos (SPF) de 1 día de edad hasta los
59 días de edad.
Diseño Experimental
Las aves fueron distribuidas en 3 grupos tratamiento de 20 aves cada uno: T1 (dosis completa de 0.3 mL), T2 (media dosis de 0.15 mL), T3 (cuarto de dosis de 0.075 mL), y un grupo control de 10 aves, T4 (no vacunado). La vacunación se dio a los 21 días por vía
intramuscular.
Desafío viral
A los 17 días post vacunación, todos los grupos fueron desafiados por vía intramuscular con 100 µL de un inóculo conteniendo un virus patógeno de la ENC, cepa velogénica con un título de 106 DIE .
y 20 % respectivamente, mientras que en T1 estuvieron ausentes. Las aves del grupo T3 presentaron un ave muerta representando el 5% de mortalidad al día 4 post infección, el grupo T4 presentó mortalidad del 100% a los 6 días post desafío, mientras que el grupo T1 y T2 no presentaron mortalidad.
Figura 1. Presentación de severa diarrea acuosa y verdosa en grupo T4.

Protección vacunal
Cuadro 1. Porcentaje de protección a la mortalidad por ENC.
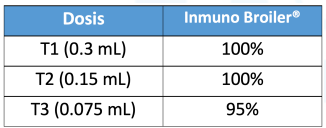
Cuadro 2. Porcentaje protección a las secuelas nerviosas.
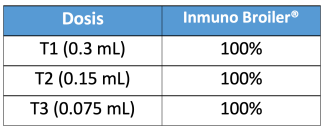
Parámetros de evaluación
Se evaluó en forma diaria la mortalidad, lesiones y signos clínicos de las aves desafiadas durante los siguientes 21 días posteriores al desafío. Asimismo, los niveles de anticuerpos fueron medidos por la prueba de inhibición de la hemaglutinación (IH) y la
prueba de ELISA previo al desafío
RESULTADOS
Signos clínicos y mortalidad
A partir del día 3 post desafío se observaron signos clínicos característicos de la ENC en las aves del grupo control no vacunado y desafiado, los mismos que se caracterizaron por depresión, diarrea, signos respiratorios y signos nerviosos. Previo a la muerte, el 30% de aves de este grupo mostraron tics nerviosos y tortícolis, como también diarrea verdosa severa durante la etapa aguda de infección (4 a 6 días) (Figura 1). Los signos respiratorios estuvieron presentes en las aves de los grupos T4, T3 y T2 en 35%, 20% y 20%
Serología
Cuadro 3. Titulación de anticuerpos la prueba de ELISA.
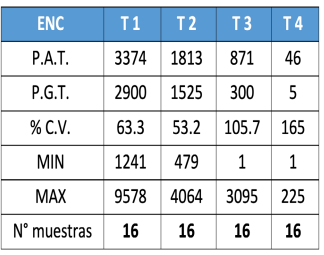
Cuadro 4. Titulación de anticuerpos por la prueba de inhibición de IH
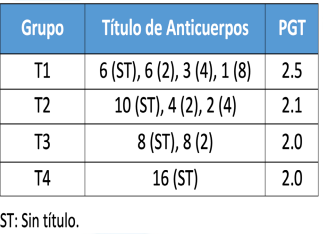
CONCLUSIONES
Las tres dosis de la vacuna Inmuno Broiler® utilizadas, cumplieron con el porcentaje de protección mínimo establecido por OIE para las vacunas inactivadas gelificada contra la Enfermedad de Newcastle.
INTRODUCCIÓN
Salmonella enterica subsp. enterica coloniza el tracto digestivo de humanos y de animales. Las salmonelas paratíficas causan enfermedades infectocontagiosas zoonóticas. En los últimos años se ha reportado un incremento de las infecciones alimentarias causadas por el consumo de alimentos con estas salmonelas. Para reducir la contaminación de los huevos para consumo y la de las plantas de faena se requieren implementar medidas de bioseguridad e implementar un programa de vacunación. La aplicación de vacunas inactivadas es importante para disminuir la excreción de las salmonelas y por ende la contaminación ambiental. En este trabajo se realizaron dos ensayos de inoculación experimental de gallinas con cepas patógenas de S. Typhimurium y
- Infantis con el objetivo de probar su eficacia
OBJETIVO
Probar la eficacia de una vacuna oleosa inactivada triple para disminuir la colonización entérica, invasión de órganos y excreción de cepas patógenas de S. Typhimurium y S. Infantis.
MATERIALES Y MÉTODOS
Animales experimentales: Pollitas BB de un día de edad
Vacuna: Vacuna oleosa inactivada triple contra Salmonella enterica subs. enterica que incluye tres serovariedades: Enteritidis, Typhimurium e Infantis.
Diseño experimental: A las 8 y 11 semanas de vida se vacunaron y revacunaron por vías subcutánea
Desafío: A las 14 semanas de vida se inocularon por vía intragluvial con entre 3 y 5 x 107 UFC de
- S. Typhimurium cepa 782 (Ensayo 1) y entre 5 y 7 x 107 UFC de Infantis cepa 360 (Ensayo 2).
Muestreo: A los 3, 6, 9, 12 y 5 días post-desafío se realizaron hisopados cloacales. A los 15 días post inoculación se cultivaron los hígados, bazos y ciegos.
Figura 1. Aves pertenecientes al estudio y placa con crecimiento bacteriano.

RESULTADOS
Cuadro 1. Resumen de los resultados de hisopados cloacales
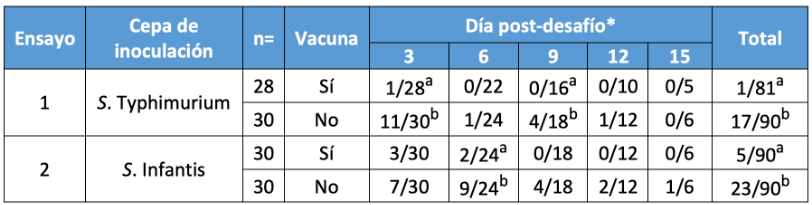
* Hisopados con aislamiento de salmonelas/hisopados totales que se muestrearon
a,b – en cada ensayo, los valores en la misma columna dentro del mismo día de muestreo o los totales con diferentes letras son significativamente diferentes p<0,05
Cuadro 2. Resumen de las sumas de los resultados de muestras de hígados, bazos y contenido de ciegos
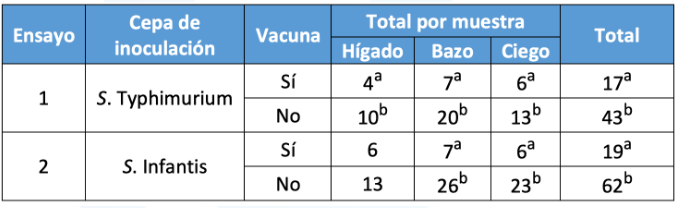
a,b – en cada ensayo, los valores en la misma columna dentro de la misma muestra o los totales con diferentes letras son significativamente diferentes p<0,05
CONCLUSIÓN
La vacuna inactivada triple contra Salmonella que incluye las serovariedades Enteritidis, Typhimurium e Infantis fue eficaz para reducir la excreción y la colonización de S. Typhimurium y S. Infantis
ANTECEDENTES
El género Salmonella incluye más de 2.400 serotipos, la salmonelosis es una enfermedad infectocontagiosa que puede desarrollarse en humanos y en animales. En los últimos años en algunos países se han incrementado los casos de infecciones alimentarias por el consumo de alimentos con Salmonella sp. Es necesario un plan de control para prevenir la infección de alimentos de origen avícola con Salmonella sp., por tal razón como medida sanitaria se debe implantar un programa vacunal para suprimir la colonización y excreción de Salmonella sp.
OBJETIVO
Evaluar el efecto protectivo (excreción, invasión y colonización) de una vacuna triple (S. Typhimurium, S. Infantis y S. Enteritidis) oleosa inactivada en gallinas ponedoras de la línea Hy-line, contra la infección experimental de Salmonella.
MATERIALES Y MÉTODOS
El estudio se llevó a cabo en los laboratorios experimentales y laboratorio de I+D de Quimtia S.A. (Lurín-Perú).
Figura 1. Metodología
Cuadro 1. Diseño experimental: distribución de aves y programa de vacunación
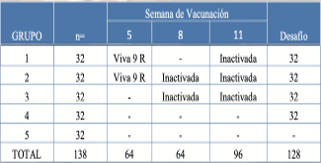
Dosis infectiva, 1 x 107 UFC por vía intragluvial de SE.
RESULTADOS
Figura 2. Resumen de los resultados de hisopados cloacales
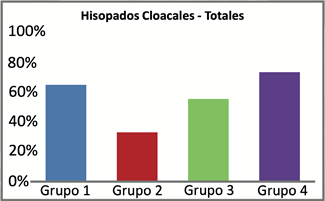
Figura 3. Resultados de muestras de órganos aislados
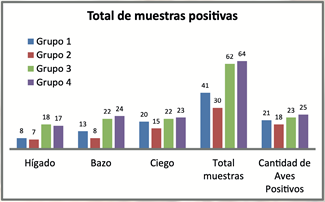
Cuadro 2. Acumulación de hisopados
cloacales positivos
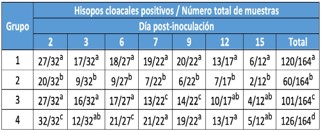
a,b,c,d Las tasas de aislamiento en la misma columna sin superíndices comunes difieren
en la Prueba de Chi2 (P<0.05).
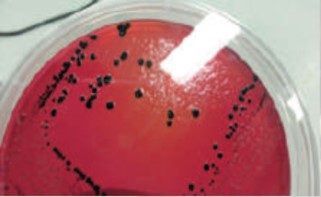
Figura 4. Crecimiento de bacterias de
Salmonella en agar XLD – Grupo 4
CONCLUSIÓN
Se redujo significativamente la invasión (hígados y bazos), colonización (ciegos) y excreción (hisopados cloacales) de Salmonella en las aves que recibieron la combinación vacunal de una o dos dosis de la vacuna inactivada con la 9R.
OBJETIVO
Evaluar la protección de las cepas de Avibacterium paragallinarum seleccionadas de los serogrupos A, B, C y B variante.
MATERIALES Y MÉTODOS
Aves
Se usaron 96 gallinas ponedoras de la línea Hy-Line de un día de edad. Las aves se dividieron en 4 grupos según la serovariedad a desafiar. Cada grupo se subdividió en 12
aves vacunadas y 12 aves control sin vacunar.
Lugar
Laboratorio de investigación aviar e investigación y desarrollo que pertenecen a QUIMTIA S.A. y están ubicados en Lurín – Lima.
Vacunación
Se vacunaron a 12 aves por grupo experimental. La inmunización se realizó a las 5 y 8 semanas de vida, mediante inyección subcutánea de 0,5 mL de la vacuna en en el tercio medio de la región dorsal del cuello.
Desafío
Las 4 cepas de Avibacterium paragallinarum serovariedades A, B, C y B var. (A. Mendoza et al., 2009; A. Mendoza et al., 2018) fueron inoculadas a las 11 semanas de vida con una dosis entre 1,9 x 107 y 6,2 x 107 UFC/mL en el seno infraorbitario izquierdo.
Signos clínicos
Al 2º y 5° día post-inoculación se registró los signos clínicos (imagen 1): Grado 0: Sin síntomas (Negativa); Grado 1: Leve conjuntivitis (Negativa); Grado 2: Conjuntivitis e hinchazón de la zona periorbital y senos paranasales; Grado 3: Conjuntivitis con el ojo parcialmente cerrado e hinchazón de la zona periorbital y senos paranasales; Grado 4: Conjuntivitis con párpados adheridos e hinchazón severa de la zona la periorbital y senos paranasales. (S. Vargas and Terzolo, 2004; Huberman et al., 2005)
Figura 1. Grados de coriza infecciosa. Interpretación de pruebas de protección del desafío de aves (Soriano-Vargas and Terzolo, 2004).

Bacteriología
Al 5° día post-inoculación se realizaron las eutanasias de todas las aves y se tomaron muestras para ver la presencia/ausencia de Av. paragallinarum en ambossenosinfraorbitarios.
RESULTADOS Y DISCUSIÓN
La sumatoria de los signos clínicos registrados de todas las aves y la presencia/ausencia de Av. paragallinarum en ambos senos infraorbitarios se puede ver en Cuadro 1. Las aves que obtuvieron valores de 0 y 1 signos clínicos se consideran negativas. Un ave se consideraba positiva si se registró signos clínicos de 2-4 o presencia de Av. paragallinarum en por lo menos un seno infraorbitario.
En general las gallinas vacunadas presentaron significativamente (prueba de Fisher, p<0,05) menor o ningún grado de lesión (signos clínicos) en comparación con las aves no vacunadas que fueron inoculadas con la misma cantidad de bacterias. Además no se aisló Av.paragallinarum de ninguna de las gallinas vacunadas.
Cuadro 1. Evaluación de signos clínicos
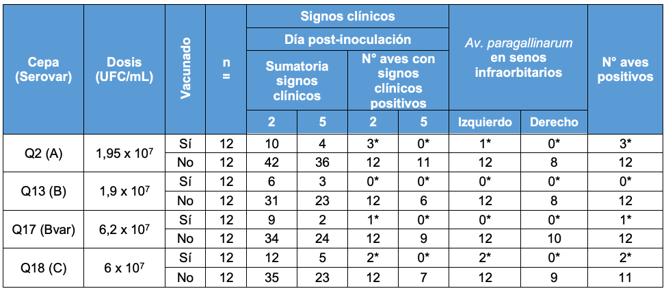
* Estadísticamente más bajo que el grupo de control no vacunado que fue desafiado con la misma cepa. Prueba exacta de Fisher p<0.05.
A- La lectura de los signos clínicos se hizo a 48 y 120 horas Post Inoculación
B- A las 11 semanas de vida se inocularon las aves en el seno infraorbitario izquierdo
CONCLUSIONES
Sumando los resultados de signos clínicos y bacteriológicos podemos indicar que la vacuna tetravalente mejorada de Coriza infecciosa aviar protege en un 100% a las aves frente a un desafío experimental con cepas de Avibacterium paragallinarum de las cuatro serovariedades A, B, C y B variante.
OBJETIVO
Determinar y optimizar los componentes del medio de cultivo para Avibacterium paragallinarum mediante el uso del diseño estadístico de Plackett-Burman y el diseño de superficie de respuesta (RSM). Además de optimizar el pH, agitación, microaerofilia y estrés oxidativo a nivel de bioreactor, y alcanzar concentraciones de 1 x1010 UFC/mL de cultivo.
MATERIALES Y MÉTODOS
Las cuatro cepas de Av. paragallinarum (A, B, C y Bvar) se reactivaron en placas de Agar Sangre Equina Hemolizada en microaerobiosis a 37°C durante 24 horas. Para la optimización de la concentración de nutrientes se usó el diseño de “Box Behnken”, para definir las concentraciones óptimas de los factores de crecimiento seleccionados se trabajó con 3 niveles alto (+1), medio (0) y bajo (-1). Finalmente, se usó un análisis de varianza para la biomasa formada y un diagrama de Pareto.
RESULTADOS
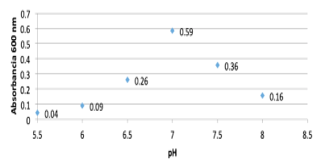
Optimización de pH
Figura 1: Efecto de distintos valores de pH en el crecimiento de Avibacterium paragallinarum
Pruducción de Biomasa de Avibacterium paragallinarum
A una concentración inicial de 0.102 Abs. 600 nm, se observa una curva típica de crecimiento alcanzando valores de 1x 1010 UFC/mL durante las 8 primeras horas de cultivo (Figura 2 y 3).
Figura 2: Curva de crecimiento típico de Avibacterium paragallinarum
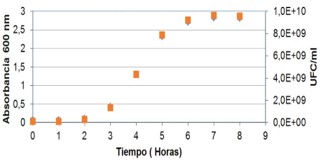
Figura 3. Crecimiento de Av. paragallinarum en medio de
cultivo optimizado en bioreactor de 0.5 mL (1), y bioreactor de 20 L (2 y 3).

Optimización de agitación y aireación
Cuadro 1. Efecto de distintas velocidades de agitaciones y aireaciones en bioreactor 0.5 L.
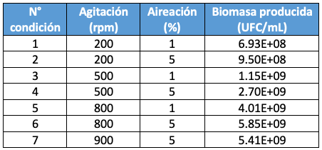
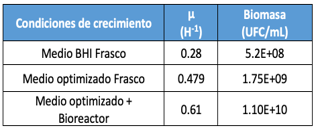
En la fase exponencial se obtuvo una velocidad especifica máxima de crecimiento tres veces mayor (0.61) a comparación de la velocidad de crecimiento en los frascos (0.28)
Condiciones de crecimiento
Cuadro 2: Producción de Biomasa en distintas condiciones de crecimiento
DISCUSIÓN
El diseño Box Behnken es un diseño de superficiederespuesta. Bajoestascondiciones teóricas se produjo 9.85×109 UFC/mL. Los valores predichos por el modelo estuvieron de acuerdo a los resultados obtenidos, por lo que la biomasa producida (1.12×1010 UFC/ mL) fue mayor que la predicha.
Se establecieron que las condiciones de crecimiento de 37 °C (dato teórico), pH de 7.1, aireación de 5% y una agitación de 200 rpm a 800 rpm, y condiciones de microaerofilia fueron importantes para el crecimiento en el medio de cultivo. Cuando la generación de especies reactivas de oxígeno supera a los mecanismos de inactivación, se presenta el estado metabólico de estrés oxidante que se caracteriza por daños moleculares y celulares (Ivana & paulina 2012). El ácido cítrico se adicionó al medio de cultivo para prevenir el estrés y favorecer el cultivo. El estrés hidrodinámico creado por velocidades de agitación superiores a 900 rpm tuvo un efecto
adverso sobre la formación de biomasa.
CONCLUSIÓN
Se produjo una alta concentración de Biomasa de Avibacterium paragallinarum utilizando metodologías estadísticas de optimización y el uso de bioreactor para el control de los parámetros de crecimiento. A 800 rpm se obtuvo la mejor transferencia, por lo que bajo estas condiciones no se presentaron limitaciones y se pudo alcanzar concentraciones máximas de 1×1010 UFC/mL en menos de 7 horas de cultivo.
OBJETIVOS
Seleccionar 4 cepas virulentas de las 4 serovariedades de Avibacterium paragallinarum A, B, C y B variante para la elaboración de una nueva bacterina contra la coriza infecciosa de las aves.
MATERIALES Y MÉTODOS
Aves
Se usaron 2200 gallinas de la línea Hy-Line a partir del primer día de vida.
Se estudiaron un total de 32 aislamientos provenientes de explotaciones avícolas de distintas regiones del Perú (A. Mendoza et al., 2009; A. Mendoza et al., 2018)
Lugar
Laboratorio de investigación aviar e investigación y desarrollo que pertenecen a QUIMTIA S.A., Lurín, Lima.
Pruebas
Se realizaron 3 series de ensayos para conocer diferentes aspectos de la patogenicidad de los aislamientos (Sandoval and Terzolo, 1997): Patogenicidad: Determinar la capacidad de las cepas de producir signos clínicos en ambos senos infraorbitarios después de inoculación experimental en el seno infraorbitario izquierdo.
Difusibilidad: Determinar la capacidad de infección horizontal a través del contagio entre aves infectados artificialmente y sanas alojadas en una misma caseta experimental. Septicemia: Determinar la capacidad de invasión de las cepas en órganos blancos (hígado, pulmones, bazo, seno paranasales e infraorbitarios).
Desafío
Las cepas de Av. paragallinarum de las
4 serovariedades A, B, C y B var. fueron inoculadas en el seno infraorbitario izquierdo.
Signos clínicos
Al 2º y 5° día post-inoculación se registró los signos clínicos (imagen 1): Grado 0: Sin síntomas (Negativa); Grado 1: Leve conjuntivitis (Negativa); Grado 2: Conjuntivitis e hinchazón de la zona periorbital y senos paranasales; Grado 3: Conjuntivitis con el ojo parcialmente cerrado e hinchazón de la zona periorbital y senos paranasales; Grado 4: Conjuntivitis con párpados adheridos e hinchazón severa de la zona la periorbital y senos paranasales (S. Vargas y Terzolo, 2004; Huberman et al., 2005).
Figura 1: Grados de coriza infecciosa. Interpretación de pruebas de protección del desafío de aves (Soriano-Vargas y Terzolo, 2004).

Bacteriología
Al 5º día se realizaron las eutanasias de todas las aves y se tomaron muestras para ver la presencia/ausencia de Av. paragallinarum en ambos senos infraorbitarios.
Para la prueba de septicemia se recolectaron los hígados de las aves infectadas con las cepas más patógenas según las puntuaciones de patogenicidad y difusibilidad. Los hígados se sembraron e incubaron en Agar Columbia Sangre al 7% por 48 horas a 37°C en jarra de anaerobiosis.
RESULTADOS Y DISCUSIÓN
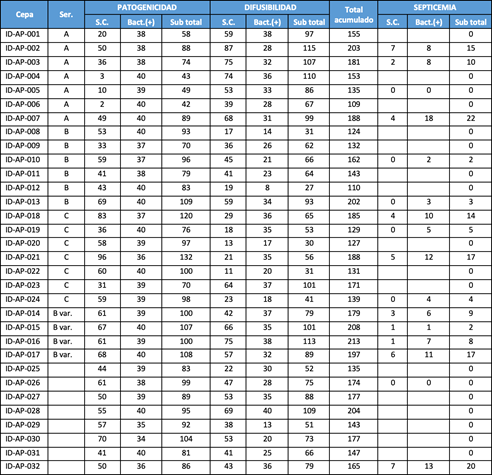
Se sumaron los resultados obtenidos por cada cepa según las pruebas de patogenicidad, septicemia y difusibilidad. En las pruebas de septicemia se usaron algunas de las cepas que fueron clasificadas como patógenas en las pruebas de patogenicidad y difusibilidad.
Cuado1. Resultados de Patogenicidad, septicemia y difusibilidad
CONCLUSIONES
De acuerdo a estos resultados, se seleccionaron como patógenas las cepas ID-AP-002 para el serovar A, procedente del Pachacámac – Lima (2006), ID-AP-013 para el serovar B procedente de Chancay – Lima (2010), ID-AP-018 procedente del departamento de San Martín (2003), e ID-AP-021, procedente de la ciudad de Quillacollo – Bolivia (2008) para el serovar C, ID-AP-017 para el serovar B variante, procedente del departamento de Arequipa (1999). Estas cepas son candidatas para la elaboración de una bacterina contra la coriza infecciosa de las aves.