MATERIALES Y MÉTODOS
Diseño del estudio
Estudio observacional descriptivo. Con el fin de identificar molecularmente el gen de la fibra para los serotipos FAdV-4, 8b y 11 de FAdV-I en muestras positivas a HCI, se estandarizó la técnica de PCRm a partir del diseño de cebadores específicos para cada serotipo.
Recolección de muestras
Se trabajaron 30 muestras de hígados de embrión de pollo con diagnóstico compatible a HCI. Las muestras estuvieron almacenadas a -20°C y provinieron de un criobanco del laboratorio de Investigación y Desarrollo de Quimtia S.A. Se obtuvieron después de pasajes en huevos libres de patógenos específicos (SPF) a partir de aislados de hígado de pollo con diagnóstico a HCI (mediante histopatología), los cuales fueron recolectados entre 1998 al 2021 procedentes de diferentes zonas de Perú. Las aves reportaron depresión severa, pérdida de peso, disminución de la conversión alimenticia; además de presentar hepatomegalia y petequias distribuidas en el hígado durante la necropsia.
Para la optimización de la PCRm se utilizaron tres muestras previamente identificadas como FAdV-4, 8b y 11 mediante secuenciamiento en base al gen del hexón en el Poultry Diagnostic and Research Center (PDRC) de la Universidad de Georgia en EEUU.
Extracción de ADN genómico/viral (ADNg)
La extracción de ADN genómico se realizó a partir de 0.25 mg de muestras de hígado de embrión de pollo utilizando el kit de extracción comercial PureLink Genomic DNA mini kit (Invitrogen-Thermo Scientific, EEUU) y siguiendo las recomendaciones del
fabricante. La concentración de ADN y pureza se determinó por espectrofotometría usando el NanoDrop One C (Thermo Scientific, EEUU). Las muestras fueron dispuestas en alícuotas y conservadas a -20°C hasta su uso.
Diseño de cebadores para la PCRm
In silico, mediante el programa informático Basic Local Alignment Search Tool (BLAST) de la base de datos del National Center for Biotechnology Information (NCBI) se seleccionaron las secuencias idénticas a la secuencia problema (query sequence) de la fibra y fibra 1 de FAdV. Se recopiló en formato FASTA la información de 83 secuencias, siendo 49 secuencias de la fibra 1 para FAdV-4, 18 y 16 secuencias de la fibra para los serotipos FAdV-8b y FAdV-11, respectivamente (Anexo 1). Las secuencias se sometieron a un alineamiento múltiple mediante el programa Clustal Omega (v. 2.0.12) para diseñar los cebadores (sentido y antisentido) de regiones variables entre los serotipos FAdV-4, 8b y 11, aunque de regiones conservadas para su serotipo diana. Se tuvieron en cuenta los siguientes parámetros: número de nucleótidos o longitud (20 a 25), temperatura de Fusión (TF) (50-60°C), porcentaje de nucleótidos Guanina y Citosina (GC%) (40- 60%). Además, con el programa Oligo Calc (Oligonucleotide Properties Calculator) se evaluó la auto complementariedad y formación de estructuras secundarias de los cebadores. Finalmente, las secuencias de los cebadores se enviaron a sintetizar a un laboratorio externo (Integrated DNA Laboratory, EEUU).
Evaluación de la especificidad de los cebadores
In silico
Cada par de cebadores diseñados fueron sometidos a un análisis por BLAST nucleótidos (Rodriguez et al.,2018) para evaluar el porcentaje de identidad del serotipo al que pertenecen dentro de la base de datos del NCBI.
PCR convencional individual
A partir de las muestras de ADN identificadas previamente por secuenciamiento como serotipos FAdV-4, 8b y 11 se evaluó la especificidad de los cebadores sintetizados mediante la amplificación de los fragmentos esperados para cada serotipo. Para optimizar las condiciones de la PCR, se realizaron dos reacciones usando el PCR Master Mix 2x (Promega corporation, EEUU); la primera con 7.14 µM de concentración final de cebadores a dos distintas temperaturas de alineamiento (Ta) a 52 y 54°C (debido a la temperatura de fusión o melting más baja de los cebadores menos 5°C), y la segunda condición con 0.7 µM de concentración final de cebadores a una Ta de 54°C (Anexo 2, 3). Ambas reacciones se trabajaron con 40 ciclos en las condiciones del termociclador (Anexo 4). Luego, cada juego de cebadores se enfrentó a las tres muestras pertenecientes a cada serotipo para evaluar su especificidad, tomando en cuenta las condiciones de PCR del Anexo 3 y 4 (54°C de Ta). Las reacciones se realizaron en el termociclador T100 (Bio Rad, EEUU). Un control negativo se colocó en cada ensayo conteniendo agua ultrapura o libre de nucleasas en lugar de ADN.
Optimización de la PCRm empleando ADN genómico/viral
Se sometieron las condiciones optimizadas de la PCR convencional empleando los tres juegos de cebadores y los tres ADN templados (FAdV-4, 8b y 11) en una sola reacción. Para ello, se incrementó el volumen de PCR Master Mix 2x debido a la adición de componentes (Anexo 5). Se siguió la programación de termociclador del Anexo 6.
Adición de MgSO4 a diferentes temperaturas de alineamiento
Para obtener mejor eficiencia de la reacción se adicionó 3.77 µM de MgSO4 (Anexo 7) y; se realizó una gradiente de la temperatura alineamiento en la programación del
termociclador (Anexo 8) debido a las diferentes temperaturas de fusión de los juegos de cebadores detallados en el Anexo 11.
Tiempo de extensión y número de ciclos
Con el fin de eliminar la presencia de bandas inespecíficas y dímeros, se disminuyó el tiempo de extensión a 1 minuto y 30 segundos (tiempo promedio de extensión de acuerdo al tamaño de los fragmentos de la fibra) y, se redujo el número de ciclos a 20. De esta manera, las condiciones estandarizadas para la reacción de PCRm de una sola muestra de ADN se muestran en el Anexo 9, mientras que las condiciones del termociclador se describen en el Anexo 10.
Detección de los productos amplificados
Los productos fueron separados por electroforesis en 0.9% de gel de Agarosa (Cleaver Scientific, Reino Unido) sumergido en buffer Tris-acetate-EDTA (TAE) (Cleaver Scientific, Reino Unido) a una concentración de 1X a 120 voltios por 70 minutos. Se empleó el colorante SYBR Safe DNA gel stain (Invitrogen-Thermo Scientific, EEUU) en una proporción 1:10000 en el gel, mientras que el colorante de carga 6X TriTrack DNA Loading Dye (Invitrogen-Thermo Scientific, EEUU) se empleó a una relación de 1:5 con cada producto de PCR. Se utilizó como marcador de peso molecular al 1Kb Opti-DNA Marker (Applied Biological Materials Inc., Canadá). Transcurrido el tiempo mencionado se visualizó en el transiluminador la positividad del gen amplificado mediante la presencia de una banda brillante del tamaño que le correspondiera según el serotipo.
Desarrollo de controles positivos con ADN plasmídico (ADNp)
Purificación del ADN a partir del gel de agarosa
Los productos de ADN obtenidos para cada serotipo se extrajeron y purificaron a partir del gel de agarosa mediante el kit Zymoclean Gel DNA Recovery (Zymo Research, EEUU), siguiendo las recomendaciones del fabricante.
Clonación y transformación
Con la finalidad de tener a disposición constante las secuencias de cada serotipo viral amplificado, se procedió al clonamiento de éstas en un sistema bacteriano. Se utilizó el vector TOPO TA cloning kit for subcloning (Invitrogen–Thermo Scientific, EEUU), siguiendo las sugerencias del fabricante. Seguidamente, se realizó el proceso de transformación por choque térmico con las células competentes de Escherichia coli DH5 alfa (Invitrogen–Thermo Scientific, EEUU). Las bacterias se sembraron en agar LB (Sigma-Aldrich, EEUU) conteniendo ampicilina, IPTG y X-gal para realizar la técnica de cribado azul/blanco (visualización de colonias blancas con inserto de secuencias amplificadas, y colonias azules sin inserto). Se seleccionaron las colonias blancas conteniendo a los clones de ADN plasmídico (ADNp) para elaborar la MASTER PLATE (placa maestra con clones de trabajo). Posteriormente, mediante el kit GenElute Plasmid Miniprep (Sigma-Aldrich, EEUU) se purificó el ADNp, verificando su correcta extracción al visualizar las diferentes formas del plásmido (superenrollado, circular, linear) en electroforesis. en una electroforesis.
Digestión con enzimas de restricción
Para corroborar que los insertos esperados de las secuencias de FAdV 4, 8b y 11 se encuentren integrados en los plásmidos obtenidos, se empleó la enzima ECO RI (Thermo Scientific, EEUU) según las indicaciones del fabricante. Al término del procedimiento se
realizó una electroforesis de los plásmidos digeridos en donde se evaluó la presencia de dos bandas, una del tamaño del vector (3.9 kbp) y la otra correspondiente al tamaño del del inserto de la fibra según el serotipo.
Secuenciamiento por el método de Sanger
Los ADN plasmídicos provenientes de la clonación de productos de PCR, se secuenciaron en la empresa Macrogen (Seúl, Corea). Mediante BLAST nucleótidos se verificó el porcentaje de identidad del fragmento amplificado frente a las secuencias del serotipo al que pertenecen dentro de la base de datos del NCBI.
Sensibilidad de la PCRm
Para conocer el límite de detección de la PCRm, se realizaron diluciones seriadas (1:10) de las tres muestras de ADN genómico trabajadas, y de las tres muestras de ADN plasmídico desarrolladas. Bajo las condiciones del Anexo 7, se preparó la primera reacción con una concentración final de cada ADN de 11.32 ng/uL y, posteriormente se realizaron 8 diluciones seriadas hasta alcanzar una concentración final para cada ADN de
11.32 x 10-8 ng/uL. Las condiciones del termociclador se encuentran descritos en el Anexo 10.
Especificidad de la PCRm
Para conocer la capacidad de la PCRm de solo detectar y diferenciar FAdV-4, 8b y 11, se prepararon reacciones empleando el ADN de otros virus aviares: virus de la enfermedad de Newcastle (NDV), virus de la bursitis infecciosa (IBDV), virus de la laringotraqueítis infecciosa (ILTV), Adenovirus aviar grupo III (FAdV-III), y los serotipos FAdV-7 y 9 de FAdV-I. Se utilizó como control positivo el ADNp obtenido de cada serotipo.
Evaluación de las muestras de HCI mediante la PCRm
Se realizó una reacción de la PCRm optimizada para cada muestra de ADNg; mientras que la reacción del control positivo empleó los tres ADNp desarrollados en simultáneo. Las condiciones de la PCRm y termociclador se describen en los Anexos 9 y 10. La concentración final de cada ADNg estuvo dentro del rango de 7.54-15.09 ng/µL y, la concentración empleada para cada ADNp fue de 11.32 x 10-3 ng/ µL o 11.32 pg/ µL.
Por otro lado, los 30 aislados diagnosticados por histopatología como HCI fueron enviados a secuenciamiento en base al gen del hexón (prueba de referencia) en el PDRC para la identificación de su serotipo.
Análisis de los datos
Cada producto amplificado de las muestras del criobanco se compararon con los controles plasmídicos para identificar a qué serotipo de FAdV-I pertenecieron. Asimismo; se compararon estos resultados con los obtenidos por secuenciamiento del hexón, determinándose en una tabla la sensibilidad de la técnica optimizada (PCRm basado en la fibra) frente a la prueba de referencia (secuencimiento basado en el hexón).
RESULTADOS
Extracción de ADN genómico/viral
Las concentraciones de ADNg dieron entre 200 a 500 ng/µL por espectrofotometría, confirmando su pureza con una relación de absorbancia A260/280 entre 1,8-2,0. Para su uso en las reacciones de PCR se llevaron a una concentración dentro del rango de 100 a 200 ng/uL.
Diseño de cebadores para la PCRm
In silico se obtuvieron las secuencias de los cebadores sentido y antisentido para cada serotipo de FAdV-I (Cuadro 1). Los parámetros de cada cebador según el laboratorio de origen se muestran en el Anexo 10.
Cuadro 1. Cebadores diseñados para la identificación de los serotipos de FAdV-I
| Serotipo | Gen | Nombre | Secuencias | Posición | Producto(pb3) |
|
FAdV-4 |
Fibra 1 |
Ad4S1
Ad4A2 |
5´GTACCTTTGGAG GGTGCGA 3´
5´CGTTGGGGGAGT AGACGTAACCCT 3´ |
87-107
1253-1276 |
1186 |
|
FAdV-
8b |
Fibra |
Ad8bS1
Ad8bA2 |
5´GTTGATGATGTC GACTGGGAGTTA 3´ 5´TGCGGAAGGTCC CTTGTATCTC 3´ |
460-484
1416-1438 |
978 |
|
FAdV- 11 |
Fibra |
Ad8bS1
Ad8bA2 |
5´ATGGGACAGCAC TCCAGCCGAA 3´
5´ACAGGAGTAGAA AAGGGTCCGAT 3´ |
31-53
1663-1686 |
1655 |
1 sentido 2antisentido 3pares de bases
Evaluación de la especificidad de los cebadores
In silico
Mediante el análisis por BLAST de nucleótidos, se verificó la especificidad de cada juego de cebadores con sus correspondientes secuencias dianas. Se obtuvo un porcentaje de identidad entre 90-100% entre serotipos de su misma especie, sin interferencia con otras especies de Adenovirus aviar u otros virus aviares.
PCR convencional individual
La primera reacción de PCR con una concentración final de cebadores de 7.14 µM y a dos distintas Ta (52°C y 54°C), mostró por electroforesis la amplificación de los fragmentos esperados para cada serotipo (Figura 1). No se observó diferencias entre las Ta, por lo que la segunda reacción se trabajó con una Ta a 54°C debido a ser la temperatura más cercana a la temperatura de fusión de los cebadores de FAdV 4 y 11. Asimismo, al disminuir la concentración final de los cebadores de 7.14 µM a 0.7 µM, se observó una mejor eficiencia de los productos amplificados y una disminución en la cantidad de dímeros (Figura 2). Finalmente, con las condiciones de la segunda reacción, se evaluó la especificidad de los cebadores para cada serotipo (Figura 3). La electroforesis
reveló los productos esperados para cada serotipo, los cebadores Ad4S y Ad4A amplificaron un producto de 1186 pb perteneciente a FAdV-4, pero no amplificaron los productos para las muestras de los serotipos FAdV-8b y 11. El par de cebadores Ad8bS y Ad8bA amplificaron un producto de 978 pb aproximadamente para FAdV-8b y no amplificaron para FAdV-4 y 11. Por último, el par de cebadores Ad11S y Ad11A amplificaron un producto de 1655 pb para la muestra FAdV-11 pero no para FAdV-4 y 8b. Los resultados obtenidos determinaron que los cebadores diseñados fueron específicos para cada serotipo.
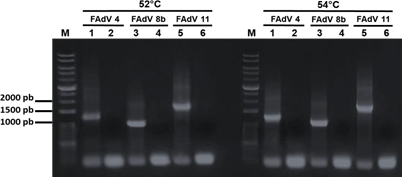
Figura 1. Electroforesis de la PCR con Ta de 52 y 54°C, concentración final de cebadores a 7.14 µM. M: marcador; carril 1: muestra FAdV-4; carril 2: control sin ADN; carril 3: muestra FAdV-8b; carril 4: control sin ADN; carril 5: muestra FAdV-11; carril 6: control sin ADN.
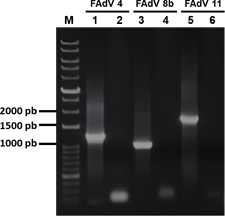
Figura 2. Electroforesis de la PCR con Ta de 54°C, concentración final de cebadores a
0.7 µM. M: marcador; carril 1: muestra FAdV-4; carril 2: control sin ADN; carril 3: muestra FAdV-8b; carril 4: control sin ADN; carril 5: muestra FAdV-11; carril 6: control sin ADN.
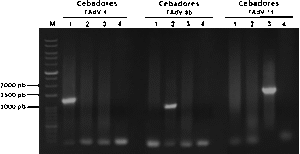
Figura 3. Electroforesis de la PCR para evaluar especificidad de los cebadores. M: marcador; FAdV-4: PCR con cebadores de FAdV-4; FAdV-8b: PCR con cebadores de FAdV-8b; FAdV-11: PCR con cebadores de FAdV-11. Carril 1: muestra FAdV-4; carril 2: muestra FAdV-8b; carril 3: muestra FAdV-11; carril 4: control sin ADN.
Optimización de la PCRm empleando ADN genómico/viral
Al emplear las condiciones del Anexo 5 y 6, en la Figura 4a se visualizó dos amplicones intensos pertenecientes a FAdV-4 y 11. Sin embargo, no se logró observar el tercer amplicón correspondiente al FAdV-8b a la temperatura de alineamiento a 54°C.
Adición de MgSO4 a diferentes temperaturas de alineamiento
Al adicionar MgSO4 se mejoró la visualización de los amplicones, siendo estos más definidos y sin presencia de barrido. A la Ta de 51°C se logró observar los tres amplicones esperados intensos y definidos, aunque aparecieron bandas inespecíficas entre los 400 y
600 bp (Figura 4b). En la PCRm con 54°C de Ta se observó amplicones definidos e intensos de FAdV-4 y 11, mientras que el amplicón de FAdV-8b se presentó tenue. Nuevamente, se observa una banda inespecífica de 400 pb (Figura 4c). A una Ta de 57°C solo se observó los amplicones pertenecientes a FAdV-4 y 11, mientras que la banda inespecífica se presentó tenue (Figura 4d). Estos resultados mostraron que a Ta de 51°C se obtuvo los tres amplicones más definidos comparados a las otras dos Ta. Aunque, con presencia de bandas inespecíficas y dímeros.
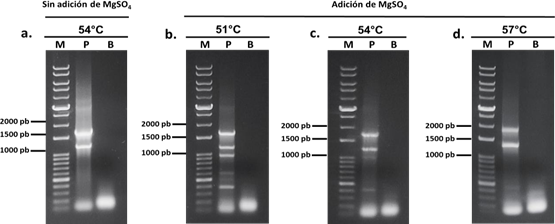
Figura 4. Electroforesis de la PCRm sin adición de MgSO4 y con adición de MgSO4 a diferentes temperaturas de alineamiento. M: marcador; P: PCRm con tres templados (FAdV-4, 8b y 11); B: control sin ADN.
Tiempo de extensión y número de ciclos
Para eliminar las bandas inespecíficas y los dímeros se disminuyó el tiempo de extensión y el número de ciclos manteniendo la Ta de 51°C. Bajo estas condiciones se observó la desaparición de las bandas inespecíficas entre los 400-600 pb, y una evidente disminución de la cantidad de dímeros (Figura 5).
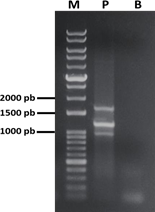
Figura 5. Electroforesis de la PCRm a menor tiempo de extensión y menor número de ciclos. M: marcador; P: PCRm con tres templados (FAdV-4, 8b y 11); B: control sin ADN.
Desarrollo de controles positivos con ADN plasmídico
Purificación del ADN a partir del gel de agarosa
A partir de la electroforesis de la Figura 3, se obtuvieron los amplicones para FAdV-4, 8b y 11, los cuales se extrajeron del gel para su purificación.
Clonación y Transformación
Luego del proceso clonación/transformación se diferenció colonias blancas de clones con vector, a partir de las cuales se realizó un banco maestro de clones que se conservaron a
-20°C. A partir de éstos, se extrajeron los ADNp de cada serotipo verificando su correcta purificación al visualizar las distintas formas del plásmido en la electroforesis (Figura 6).
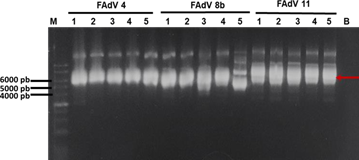
Figura 6. Electroforesis de plásmidos purificados con el inserto amplificado según cada serotipo. M: marcador; FAdV-4: plásmidos de FAdV-4; FAdV-8b: plásmidos de FAdV- 8b; FAdV-11: plásmidos de FAdV-11. B: control sin ADN. Flecha roja: formas del plásmido.
Digestión con enzimas de restricción
Mediante la digestión de los plásmidos con la enzima ECO RI, se comprobó la presencia de los insertos del fragmento de la fibra y la banda perteneciente al resto del vector (Figura 7). La enzima cortó a los extremos del inserto en el vector TOPO TA (3.9 kb) brindando dos fragmentos: uno correspondiente al tamaño del inserto (FAdV-4: 1186, 8b: 976 y 11: 1655) y otro correspondiente al tamaño del resto de bp del vector.
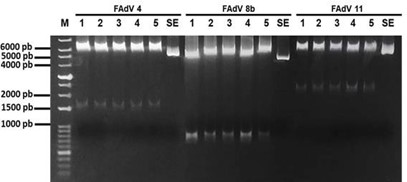
Figura 7. Electroforesis de la digestión enzimática de los plásmidos conteniendo la secuencia de FAdV según cada serotipo. M: marcador; FAdV-4: plásmidos de FAdV-4;
FAdV-8b: plásmidos de FAdV-8b; FAdV-11: plásmidos de FAdV-11. SE: control negativo (plásmido sin enzima).
Secuenciamiento por el método de Sanger
Los productos de la fibra y fibra 1 clonados y secuenciados a partir de los plásmidos de cada serotipo (FAdV-4, 8 y 11) se analizaron mediante BLAST nucleótidos. Los resultados mostraron un porcentaje de identidad de hasta 99.7% con secuencias del fragmento de la fibra anotadas en el NCBI para FAdV-4, 98% para FAdV-8b y 97.3% para FAdV-11, corroborando que cada inserto corresponde a su serotipo y especie específica.
Sensibilidad de la PCRm
En la Figura 8 se observó que el límite de detección de ADNg y ADNp de cada serotipo a partir de 11.32 ng/uL, fue a la dilución de 10-2 y10-5 respectivamente. Según lo obtenido, se puede emplear el control positivo hasta una concentración de 11.32 x 10-5 ng/uL o 0.1132 pg/uL de cada plásmido; mientras que el ADN genómico se puede emplear hasta una concentración de 11.32 x 10-2 ng/uL o 0.1132 ng/uL de cada serotipo.

Figura 8. Electroforesis para evaluar la sensibilidad de la PCRm con ADN genómico y ADN plasmídico. M: marcador; 100– 10-8: PCRm a distintas diluciones a partir de 11.32 ng/uL; B: PCRm control sin ADN.
Especificidad de la PCRm
En la Figura 9 se comprueba que la PCRm no es capaz de amplificar NDV, IBDV, ILTV, FAdV-III, ni a los serotipos 7 y 9 de FAdV-I. Por lo tanto, la técnica optimizada es específica para los serotipos FAdV-4, 8b y 11 de FAdV-I.
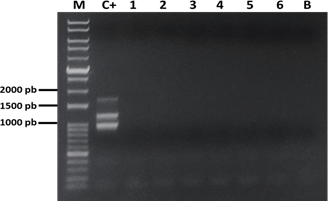
Figura 9. Electroforesis para evaluar la especificidad de la PCRm. M: marcador; C+: control positivo de ADNp, 1: NDV, 2: IBDV, 3: ILTV, 4: FAdV-III, 5: FAdV-7, 6: FAdV-9, B: PCRm control sin ADN.
Evaluación de las muestras de HCI mediante la PCRm
Se corrió los productos de PCRm de todas las muestras positivas a HCI, así como el control plasmídico (Figura 10).
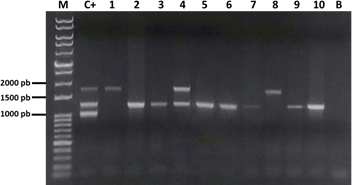
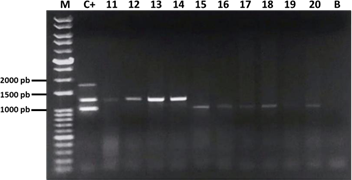
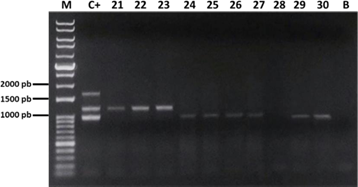
Figura 10. Electroforesis de los productos de la PCR múltiple de las 30 muestras de FAdV-I. M: marcador; C+: control positivo de ADNp; carril 1 al 30: muestras; B: control sin ADN.
Se logró caracterizar los serotipos 4, 8b y 11; de los cuales 14 muestras (46.7%) fueron positivas a FAdV-4, 12 (40%) a FAdV-8b y, dos (6.7%) a FAdV-11. Asimismo, se
observó la presencia de una coinfección entre FAdV-4 y FAdV-11 (3.3%); mientras que una muestra (3.3%) dio resultado negativo.
Posteriormente, para determinar la sensibilidad de la PCRm frente al secuenciamiento en base al hexón se compararon los resultados obtenidos de ambas pruebas diagnósticas (Cuadro 2). La muestra de coinfección entre FAdV-4 y 11 fue tomada como positiva para ambos serotipos.
Cuadro 2. Sensibilidad de la PCR multiplex frente al secuenciamiento.
|
Serotipos |
Secuenciamiento
Gen hexón |
PCR Multiplex
Gen fibra |
Sensibilidad
del PCRm (%) |
| FAdV-41 | 15 | 15 | 100% |
| FAdV-8b | 13 | 12 | 92.3% |
| FAdV-11 | 2 | 3 | 100% |
1Detección del fragmento de la fibra 1 para el caso de FAdV-4
A new law signed into effect this week requires corporations to publicly disclose their political contributions, including donations to candidates, political parties, and advocacy groups
- Lorem ipsum dolor sit amet, consectetur adipisicing elit, sed do eiusmod tempor incididunt ut labore et dolore magna aliqua. Ut enim ad minim veniam
- quis nostrud exercitation ullamco laboris nisi ut aliquip ex ea commodo consequat. Duis aute irure dolor in reprehenderit in voluptate velit esse cillum dolore eu fugiat nulla pariatur. Excepteur sint occaecat cupidatat non proident, sunt in culpa qui officia deserunt mollit anim id est laborum.
The law requires corporations to file quarterly reports detailing their political spending, which will be posted on a publicly accessible website maintained by the Federal Election Commission. Supporters of the law argue that it will help prevent undue influence by special interests in the political process, and will allow voters to make more informed decisions at the ballot box. Finally, a federal court has ruled against religious discrimination in a land use case, finding that a local government violated the rights of a religious organization by denying it permission to use its property for religious purposes. This ruling is significant for its defense of religious freedom and its emphasis on treating all individuals and organizations equally under the law.

The law requires corporations to file quarterly reports detailing their political spending, which will be posted on a publicly accessible website maintained by the Federal Election Commission. Supporters of the law argue that it will help prevent undue influence by special interests in the political process, and will allow voters to make more informed decisions at the ballot box. Finally, a federal court has ruled against religious discrimination in a land use case, finding that a local government violated the rights of a religious organization by denying it permission to use its property for religious purposes. This ruling is significant for its defense of religious freedom and its emphasis on treating all individuals and organizations equally under the law.
A new law signed into effect this week requires corporations to publicly disclose their political contributions, including donations to candidates, political parties, and advocacy groups
The law requires corporations to file quarterly reports detailing their political spending, which will be posted on a publicly accessible website maintained by the Federal Election Commission. Supporters of the law argue that it will help prevent undue influence by special interests in the political process, and will allow voters to make more informed decisions at the ballot box. Finally, a federal court has ruled against religious discrimination in a land use case, finding that a local government violated the rights of a religious organization by denying it permission to use its property for religious purposes. This ruling is significant for its defense of religious freedom and its emphasis on treating all individuals and organizations equally under the law.